چگونه یک پروتئین مرموز سلولهای عصبی را پاکسازی میکند؟
شناسایی مسیر سنتز BMP و نقش آن در تحلیل عصبی
خلاصه
برای بیش از پنجاه سال، یکی از پرسشهای بنیادین در زیستشناسی سلولی و علوم اعصاب بیپاسخ مانده بود: سازوکار مولکولی سنتز بیس(مونوآسیلگلیسرو)فسفات (BMP)، یکی از لیپیدهای کلیدی لیزوزومی، چگونه است؟ BMP نقشی اساسی در تنظیم همایستایی لیپیدها، پاکسازی چربیهای تجمعیافته و حفظ سلامت نورونها ایفا میکند. پژوهشهای اخیر نشان میدهد که پروتئین CLN5، که پیشتر صرفاً بهعنوان عامل ژنتیکی بیماری نورودژنراتیو کودکی باتن شناخته میشد، در واقع همان آنزیم گمشده مسئول سنتز BMP است. این کشف نهتنها یک معمای نیمقرنی را حل میکند، بلکه چارچوب مفهومی تازهای برای درک مکانیسمهای مشترک در بیماریهایی نظیر آلزایمر، پارکینسون و دمانس فرونتوتمپورال فراهم میآورد و مسیرهای درمانی نوینی را پیشروی پژوهشگران میگشاید.
مقدمه: لیزوزوم، مرکز تنظیم تعادل لیپیدی نورون
سلولهای عصبی برای حفظ بقا و عملکرد دقیق خود، به سامانهای کارآمد برای تجزیه و بازیافت اجزای سلولی وابستهاند. لیزوزومها بهعنوان اندامکهای کلیدی این سامانه، مسئول تجزیه ماکرومولکولها و بازیافت اجزای زیستی هستند و نقش تعیینکنندهای در سازگاری سلول با شرایط متغیر متابولیکی دارند.
اختلال در عملکرد لیزوزومها، بهویژه در مسیرهای تجزیه لیپیدها، پیامدهای پاتولوژیک گستردهای به همراه دارد. جهش در ژنهای مرتبط با متابولیسم لیپیدی لیزوزومی موجب تجمع غیرطبیعی چربیها میشود؛ پدیدهای که هم در اختلالات ذخیرهای لیزوزومی عصبی (nLSDs) در کودکان و هم در بیماریهای تحلیلبرنده عصبی بزرگسالان مانند آلزایمر و پارکینسون مشاهده میشود. این شواهد نشان میدهد که نارسایی لیزوزومی یکی از محرکهای مرکزی تحلیل عصبی است و حفظ عملکرد این اندامک، هدفی راهبردی در مداخلات درمانی به شمار میرود.
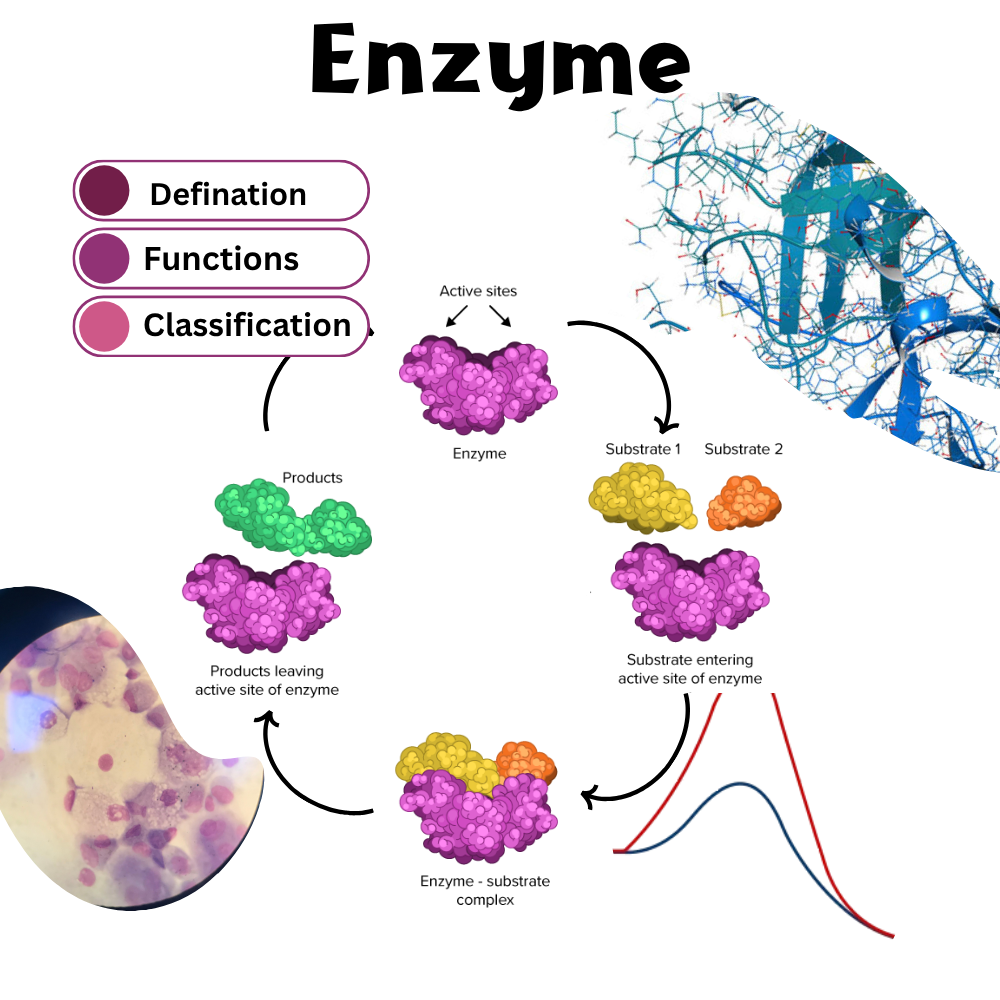
BMP: لیپید کلیدی اما ناشناخته
یکی از مهمترین ابزارهای مولکولی لیزوزوم برای پاکسازی لیپیدها، BMP یا بیس(مونوآسیلگلیسرو)فسفات است. این لیپید آنیونی با ساختار ویژه و زنجیرههای اسیل چندغیراشباع، در سطح وزیکولهای لیزوزومی تجمع مییابد و با جذب آنزیمهای هیدرولیتیک دارای بار مثبت، فرآیند استخراج و تجزیه لیپیدها را تسهیل میکند. از این منظر، BMP را میتوان بهعنوان یک تنظیمکننده فعال در همایستایی لیپیدی لیزوزومها در نظر گرفت.
با وجود نقش حیاتی BMP در سلامت سلولی، مسیر بیوسنتزی آن برای دههها ناشناخته باقی مانده بود و «سنتزکننده BMP» یکی از حلقههای مفقوده زیستشناسی لیزوزومی محسوب میشد.
تمرکز پژوهش: بیماری باتن و ژن CLN5
نقطه آغاز این پژوهش، بررسی بیماری باتن بود؛ یک اختلال نورودژنراتیو دوران کودکی که ناشی از جهش در مجموعهای از ژنها با عنوان CLN1 تا CLN14 است. تمرکز اصلی بر ژن CLN5 قرار گرفت؛ ژنی که علاوه بر ارتباط با بیماری باتن، بهعنوان عامل خطر در آلزایمر نیز گزارش شده بود، اما عملکرد مولکولی آن مشخص نبود.
با حذف CLN5 از سلولها و تحلیل ترکیب لیپیدهای لیزوزومی بهوسیله طیفسنجی جرمی، نتایجی چشمگیر بهدست آمد: میزان BMP تقریباً بهطور کامل کاهش یافت، در حالی که پیشماده آن، یعنی لیزوفوسفاتیدیلگلیسرول (LPG)، بیش از ۱۰۰ برابر افزایش نشان داد. تکرار این آزمایش در نورونهای مشتقشده از سلولهای بنیادی پرتوان انسانی (iPSC-derived neurons) اثرات شدیدتری را آشکار کرد؛ بهگونهای که BMP بهطور کامل ناپدید شد و LPG بیش از ۲۰۰ برابر انباشته گردید. این دادهها بهوضوح بر نقش اساسی CLN5 در تولید BMP دلالت داشتند.
شناسایی سنتزکننده گمشده BMP
تحلیل ساختار سهبعدی CLN5 نشان داد که این پروتئین دارای شیارهای طویل و لیپوفیلیک است که قابلیت اتصال به LPG را دارند. این مشاهده فرضیهای کلیدی را مطرح کرد: آیا CLN5 همان آنزیم مسئول سنتز BMP است؟
برای آزمون این فرضیه، CLN5 بازترکیبی در شرایط اسیدی مشابه محیط لیزوزوم با LPG واکنش داده شد. نتیجه قطعی بود BMP تولید شد. این آزمایش ساده اما تعیینکننده، نشان داد که CLN5 همان سنتزکننده ناشناخته BMP است و بدینترتیب، معمایی پنجاهساله در زیستشناسی سلولی حل شد.
پیامدهای مکانیکی و سلولی
از منظر بیوشیمیایی، CLN5 با استفاده از یک باقیمانده سیستئین نوکلئوفیل، دو مولکول LPG را به یک مولکول BMP متصل میکند. این یافته اهمیت ویژهای دارد، زیرا نشان میدهد لیزوزومها صرفاً اندامکهای تخریبی نیستند، بلکه توانایی سنتز لیپیدهای پیچیده را نیز دارند.
افزون بر این، مشخص شد که BMP میتواند بهصورت یک حلقه بازخورد مثبت، فعالیت سنتزکننده خود را تقویت کند؛ سازوکاری که به پایداری سیستم پاکسازی لیپیدی کمک میکند.
ابعاد بالینی و بیماریزا
بررسی واریانتهای بیماریزا نشان داد که جهش Asn143Ser در بیماران مبتلا به بیماری باتن، فعالیت آنزیمی CLN5 را به کمتر از ۱۰٪ کاهش میدهد. در نتیجه، سلولها قادر به تولید BMP کافی نیستند. مطالعات میکروسکوپ الکترونی نیز آشکار ساخت که در غیاب BMP، ساختار وزیکولهای لیزوزومی مختل شده و تجمع لیپیدهای سمی به مرگ سلولی میانجامد.
نتیجهگیری و چشمانداز درمانی
این یافتهها نشان میدهد که اختلال در مسیر سنتز BMP میتواند یک مکانیسم مشترک در طیف وسیعی از بیماریهای تحلیلبرنده عصبی باشد. شناسایی CLN5 بهعنوان سنتزکننده BMP، نهتنها درک ما از زیستشناسی لیزوزوم را متحول میکند، بلکه زمینه را برای توسعه راهبردهای درمانی نوین، از جمله فعالسازی مسیر BMP یا جایگزینی آنزیمی، فراهم میسازد. مسیری که سالها در تاریکی باقی مانده بود، اکنون میتواند به کلیدی برای حفاظت از میلیونها نورون و بهبود کیفیت زندگی بیماران بدل شود.
میتوان BMP را بهعنوان یک تنظیمکننده حیاتی درون سلول تصور کرد که هنگام افزایش بیش از حد لیپیدها، فرآیند پاکسازی لیزوزومی را فعال میسازد. در این چارچوب، CLN5 نقش واحد تولیدکننده این مولکول کلیدی را ایفا میکند و فقدان آن، سلول را در معرض انباشت لیپیدهای سمی و تخریب عصبی قرار میدهد.
منابع و توضیحات:
https://www.science.org/doi/10.1126/science.aec9580