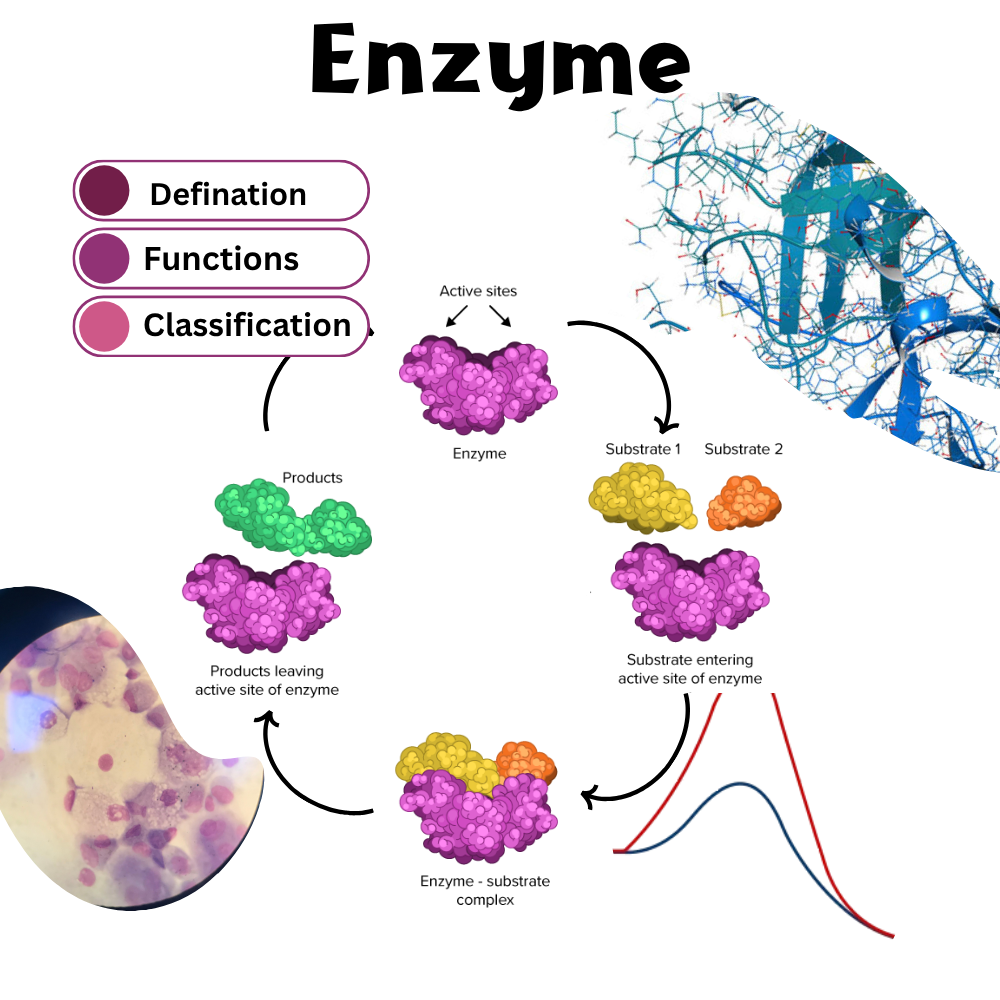
چگونه میکروروباتها دارو را دقیقاً به محل بیماری میرسانند؟
میکروروباتهای مغناطیسی در پزشکی نوین: گامی بهسوی درمانهای هدفمند و کمتهاجمی
خلاصه
پیشرفتهای اخیر در رباتیک پزشکی امکان توسعه سامانههایی را فراهم کرده است که میتوانند دارو را با دقت بالا و بهصورت موضعی در بدن انسان آزاد کنند. یکی از نوآورانهترین این رویکردها، استفاده از میکروروباتهای مغناطیسی است؛ ساختارهایی در مقیاس میکرومتر که قابلیت حرکت کنترلشده در جریان خون را دارند. در این مقاله، یک پلتفرم رباتیک سازگار با کاربردهای بالینی معرفی میشود که قادر است میکروروباتهای مغناطیسی را هدایت کرده، فرآیند آزادسازی دارو را کنترل نماید و همزمان امکان ردیابی آنها را با تصویربرداری فلوروسکوپی فراهم آورد. نتایج حاصل از آزمایشها در مدلهای شبیهسازیشده انسانی و مدلهای حیوانی بزرگ نشان میدهد که این فناوری میتواند نقش مهمی در آینده درمانهای هدفمند و کمتهاجمی ایفا کند.
چالشهای درمان دارویی و ضرورت رویکردهای هدفمند
درمانهای دارویی متداول غالباً بهصورت سیستمیک انجام میشوند؛ به این معنا که دارو پس از ورود به بدن در سراسر گردش خون توزیع میشود. این شیوه، اگرچه ساده و رایج است، اما با بروز عوارض جانبی ناخواسته همراه بوده و یکی از دلایل اصلی شکست داروها در مراحل کارآزمایی بالینی بهشمار میرود. برآوردها نشان میدهد حدود ۳۰ درصد از داروها به دلیل سمیت یا عوارض سیستمیک قادر به عبور از مراحل بالینی نیستند. این در حالی است که در بسیاری از بیماریها، از جمله تومورها یا انسدادهای عروقی، اثر درمانی مطلوب تنها در یک ناحیه محدود مورد نیاز است.
در پاسخ به این چالش، پژوهشهای دو دهه اخیر به توسعه میکروروباتها و نانوروباتهای مغناطیسی معطوف شده است. این ساختارهای ریزمقیاس میتوانند همانند حاملهای هوشمند، دارو را مستقیماً به محل آسیبدیده منتقل کرده و با افزایش غلظت موضعی دارو، اثربخشی درمان را افزایش و عوارض جانبی را به حداقل برسانند.
پیشرفتها و موانع انتقال به کاربرد بالینی
تحقیقات گستردهای در زمینه بهینهسازی حرکت، طراحی مواد سازگار با بدن (Biocompatible Materials) و روشهای ساخت میکروروباتها انجام شده است. برخی از این روباتها با الهام از حرکت سلولها و میکروارگانیسمها طراحی شدهاند و توانایی ناوبری دقیق در محیطهای زیستی پیچیده را دارند. همچنین امکان بارگذاری طیف متنوعی از داروها و ردیابی زنده آنها از طریق روشهای تصویربرداری پزشکی فراهم شده است.
با این حال، انتقال این فناوریها از آزمایشگاه به محیط بالینی با چالشهای اساسی همراه است. مواد مورد استفاده باید زیستسازگار و ترجیحاً زیستتجزیهپذیر باشند تا پس از انجام مأموریت، بدون نیاز به مداخله جراحی از بدن حذف شوند. افزون بر این، تولید میدانها و گرادیانهای مغناطیسی با شدت کافی برای هدایت دقیق روباتها در بدن انسان، به دلیل کاهش شدت میدان با افزایش فاصله، یک محدودیت فنی مهم محسوب میشود.
معرفی پلتفرم رباتیک مغناطیسی
در این پژوهش، یک پلتفرم رباتیک ویژه برای کاربردهای بالینی معرفی شده است که اجزای اصلی آن عبارتاند از:
- دو واحد الکترومغناطیسی جفتشده برای ایجاد میدانها و گرادیانهای مغناطیسی کنترلشده
- یک کاتتر اختصاصی برای آزادسازی میکروروبات
- یک میکروروبات بدون اتصال که از آن با عنوان «کپسول مغناطیسی» یاد میشود.
کپسول مغناطیسی از یک ماتریس ژلاتینی زیستسازگار تشکیل شده که نانوذرات آهن و تانتالوم در آن تعبیه شدهاند و داروی درمانی درون این ساختار محصور است. اعمال میدانهای مغناطیسی چرخشی و گرادیانی امکان هدایت کپسول را در عروق و حتی فضاهای اطراف مغز فراهم میکند. پس از حل شدن ژلاتین در ناحیه هدف، نانوذرات حامل دارو میتوانند به عروق کوچکتر نفوذ کرده و دارو را به نقاط دوردست منتقل کنند.
مکانیسمهای حرکتی میکروروبات
حرکت میکروروبات مغناطیسی بر اساس سه سازوکار اصلی انجام میشود:
- حرکت چرخشی روی دیواره رگها تحت تأثیر میدان مغناطیسی، مناسب برای نواحی با جریان خون کم مانند فضای پیرامغزی.
- کشش توسط گرادیان مغناطیسی که امکان حرکت فعال روبات در خلاف جهت جریان خون را فراهم کرده و سرعتهایی تا حدود ۲۱ سانتیمتر بر ثانیه ایجاد میکند.
- حرکت همراه با جریان خون که در آن جریان طبیعی خون عامل جابهجایی است و میدان مغناطیسی تنها مسیر دقیق حرکت را تنظیم میکند.
در آزمایشهای انجامشده در مدلهای انشعابی (Y-junction)، حدود ۹۵ درصد از کپسولها با موفقیت به شاخه هدف هدایت شدند. همچنین ردیابی لحظهبهلحظه مسیر حرکت با استفاده از فلوروسکوپی امکانپذیر بود.
کنترل آزادسازی دارو و ملاحظات ایمنی
آزادسازی دارو از میکروروبات به دو شیوه قابل انجام است:
- آزادسازی تدریجی و کنترلشده، مناسب برای درمانهای مزمن یا تومورهای کوچک
- آزادسازی سریع و متمرکز، کاربردی در شرایط اورژانسی مانند انحلال لختههای خونی
با اعمال تحریک مغناطیسی با فرکانس بالا، نانوذرات گرم شده و ماتریس ژلاتینی حل میشود. این فرآیند نهتنها موجب آزادسازی دارو میگردد، بلکه در صورت انحراف روبات به ناحیه ناخواسته، امکان غیرفعالسازی سریع آن را نیز فراهم میکند؛ مفهومی که میتوان آن را بهعنوان یک سازوکار «ایمنی اضطراری» در نظر گرفت.
یافتههای تجربی
- در مدل سهبعدی سیلیکونی عروق انسانی، میکروروبات توانست در جریانهایی با سرعت ۳۷ سانتیمتر بر ثانیه در شریان کاروتید داخلی حرکت کرده و به سه شاخه دوردست دست یابد.
- با بارگذاری داروی ترومبولیتیک rtPA، روبات موفق به انحلال لخته خون انسانی شد و جریان خون ظرف ۷٫۵ دقیقه بازگشت؛ بخش عمده لخته نیز در کمتر از ۲۰ دقیقه حل شد.
- آزمایشها در مدلهای حیوانی بزرگ (گوسفند و خوک) نشان داد هر سه روش هدایت روبات با دقت بالا و تکرارپذیری کامل قابل اجرا هستند.
اهمیت و چشمانداز بالینی
میکروروباتهای مغناطیسی این امکان را فراهم میکنند که دارو با دقت بالا به نواحی حساس بدن منتقل شود، بدون آنکه نیاز به جراحی باز یا مواجهه با عوارض داروهای سیستمیک وجود داشته باشد. این پلتفرم، تحویل هدفمند دارو را یک گام به تحقق بالینی نزدیکتر کرده و چشمانداز روشنی برای درمان تومورها، انسدادهای عروقی و عفونتهای موضعی ترسیم میکند.
میتوان جریان خون را به رودخانهای پیچدرپیچ تشبیه کرد و میکروروبات مغناطیسی را همچون قایقی بسیار کوچک که با نیروی میدان مغناطیسی هدایت میشود. این قایق مسیر خود را در میان شاخهها انتخاب میکند، به مقصد دقیق میرسد، محموله درمانی خود را تخلیه میکند و در نهایت، بدون ایجاد مانع یا آسیب، بهطور کامل حل شده و از سیستم حذف میشود.
منابع و توضیحات:
Fabian C. Landers et al.,Clinically ready magnetic microrobots for targeted therapies.Science390,710-715(2025). DOI:10.1126/science.adx1708