سرطانهای شایع در انسان
مقدمه
سرطان، یکی از پیچیدهترین و چالشبرانگیزترین بیماریهای قرن حاضر، به دلیل رشد غیرقابل کنترل سلولها و توانایی این سلولها برای تهاجم به بافتهای سالم، یکی از اصلیترین عوامل مرگ و میر در جهان محسوب میشود. این بیماری نه تنها بر سلامت جسمی بیماران تأثیر میگذارد، بلکه پیامدهای اجتماعی، اقتصادی و روانی گستردهای برای خانوادهها و جوامع به همراه دارد. با پیشرفت علم پزشکی و پژوهشهای ژنتیکی، درک ما از مکانیسمهای مولکولی سرطان و عوامل مؤثر بر شروع و پیشرفت آن بهطور چشمگیری افزایش یافته است، اما هنوز بسیاری از جنبههای این بیماری نیازمند تحقیقات بیشتر است.
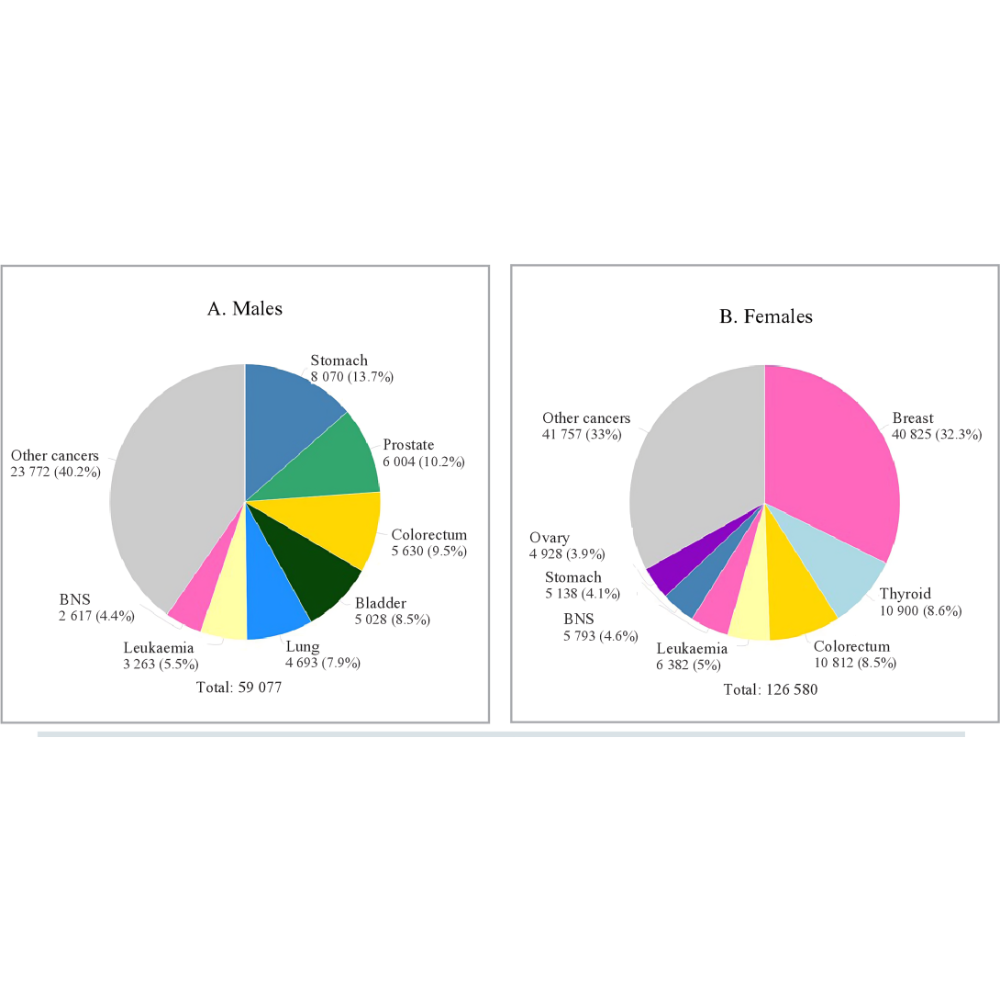
اپیدمیولوژی سرطان نشان میدهد که این بیماری با شیوع متفاوت در کشورهای مختلف و میان گروههای جمعیتی متنوع رخ میدهد. بر اساس دادههای سازمان جهانی بهداشت، سرطانها سالانه میلیونها نفر را تحت تأثیر قرار میدهند و برخی از انواع آنها، مانند سرطان ریه، پستان، روده بزرگ و کبد، سهم قابل توجهی از بار بیماریها را در سطح جهانی به خود اختصاص دادهاند. این تفاوتها معمولاً ناشی از ترکیبی از عوامل ژنتیکی، محیطی، رفتاری و سبک زندگی هستند و شناسایی این عوامل برای توسعه استراتژیهای پیشگیری و درمان مؤثر ضروری است.
عوامل متعددی در ایجاد سرطان نقش دارند و این عوامل میتوانند شامل جهشهای ژنتیکی، اختلالات اپیژنتیک، عفونتهای ویروسی و باکتریایی، مواجهه با مواد شیمیایی محیطی، تغذیه نامناسب، مصرف سیگار و الکل، چاقی و بیتحرکی باشند. به عنوان مثال، ویروس پاپیلومای انسانی (HPV) به عنوان عامل اصلی سرطان گردن رحم شناخته شده و تحقیقات جدید نشان میدهند که این ویروس میتواند در ایجاد سرطانهای دهان، حلق و حتی مثانه نقش داشته باشد. همچنین، مواجهه طولانیمدت با مواد شیمیایی مانند PFAS و فلزات سنگین، خطر ابتلا به سرطانهای گوارشی و پستان را افزایش میدهد.
یکی دیگر از جنبههای مهم در مطالعه سرطانها، نقش سیستم ایمنی و میکروبیوم بدن است. سیستم ایمنی در شناسایی و از بین بردن سلولهای غیرطبیعی نقش اساسی دارد و اختلال در عملکرد آن میتواند زمینهساز رشد تومورها شود. مطالعات اخیر نشان دادهاند که میکروبیوم روده، پوست و واژن میتواند با فرآیندهای التهابی و مسیرهای سیگنالینگ سلولی تعامل داشته باشد و بر حساسیت یا مقاومت فرد نسبت به سرطان تأثیر بگذارد. این یافتهها افق جدیدی برای تشخیص زودهنگام، پیشگیری و حتی درمانهای مبتنی بر اصلاح میکروبیوم باز کرده است.
علاوه بر این، تغییرات سبک زندگی و عوامل محیطی نقش مهمی در شیوع سرطانها دارند. رژیم غذایی سرشار از سبزیجات، میوهها و ترکیبات فیتوشیمیایی مانند کورکومین و رزوراترول میتواند اثر محافظتی در برابر برخی سرطانها داشته باشد، در حالی که مصرف غذاهای فرآوریشده، چربیهای اشباع و کمتحرکی خطر ابتلا را افزایش میدهد. این دادهها نشان میدهند که پیشگیری از سرطان تنها محدود به درمان پزشکی نیست، بلکه نیازمند اصلاح رفتارها و افزایش آگاهی عمومی نیز هست.
با توجه به اهمیت موضوع، مقاله حاضر با هدف ارائه یک مرور جامع بر سرطانهای شایع در انسان تهیه شده است. این مقاله تلاش دارد تا عوامل مولکولی، ژنتیکی، محیطی و رفتاری مؤثر بر سرطان، انواع مختلف سرطانهای شایع، روشهای تشخیص و پایش، و درمانهای نوین و آیندهنگرانه را بررسی کند. همچنین، ارتباط بین ویروسها، میکروبیوم، مسیرهای سیگنالینگ و عوامل محیطی با سرطانها به صورت علمی و دقیق تشریح خواهد شد تا هم برای متخصصان پزشکی و پژوهشگران و هم برای مخاطب عمومی قابل استفاده باشد.
در نهایت، درک کامل از علتها، پیشگیری و درمان سرطانها، نه تنها به کاهش مرگ و میر ناشی از این بیماری کمک میکند، بلکه میتواند روند تحقیقات آینده را نیز هدایت کند و زمینهساز توسعه روشهای درمانی دقیق و شخصیسازیشده شود. با توجه به پیچیدگی سرطانها و تعاملات متعدد عوامل در ایجاد و پیشرفت آنها، این مقاله تلاشی است برای ارائه تصویری جامع و علمی که بتواند نیازهای اطلاعاتی مختلف مخاطبان را پاسخ دهد.
مبانی سرطانشناسی
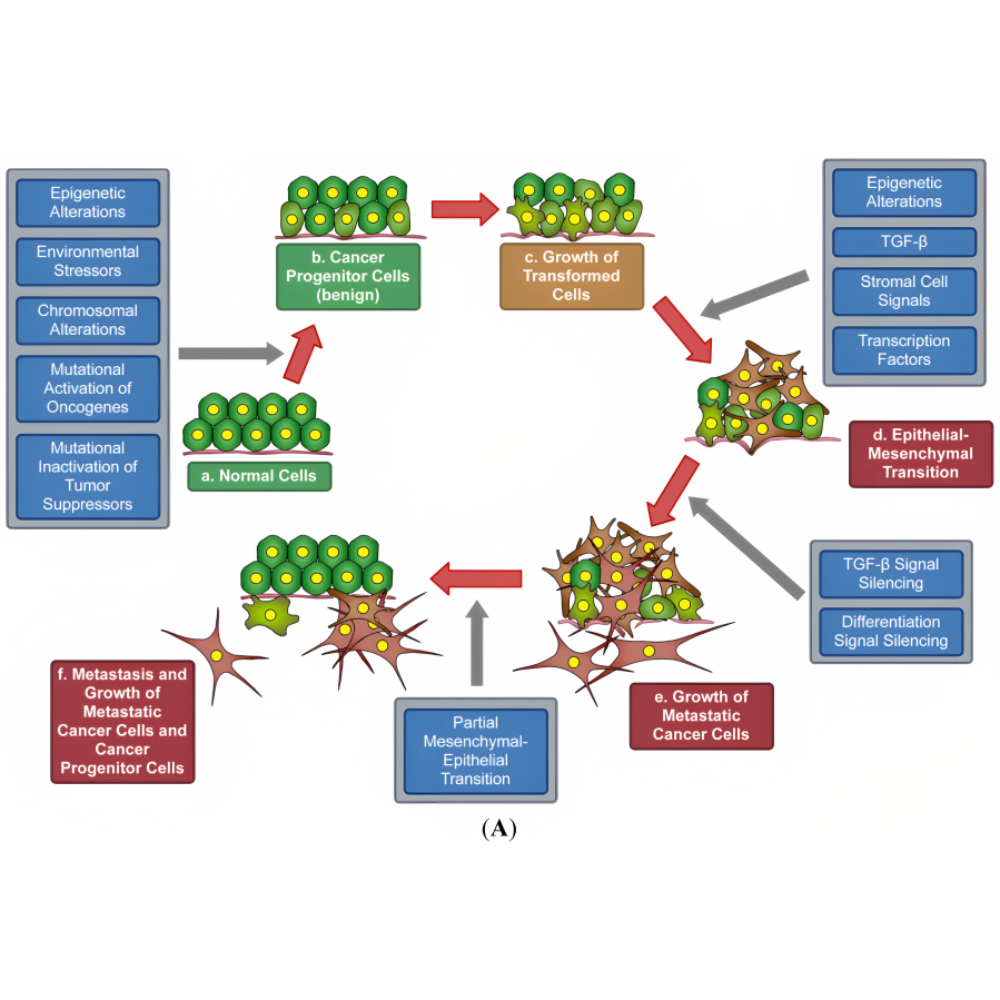
سرطان یک بیماری چندعاملی است که در آن سلولها بهطور غیرقابل کنترل تقسیم میشوند و توانایی تهاجم به بافتهای اطراف و متاستاز به سایر اندامها را پیدا میکنند. فهم این پدیده نیازمند شناخت دقیق مکانیسمهای مولکولی، تغییرات ژنتیکی و اپیژنتیکی، تعامل سلولها با سیستم ایمنی و محیط میکروبی بدن است. این بخش به بررسی این مبانی میپردازد تا پایه علمی لازم برای درک سرطانهای شایع فراهم شود.
مکانیسمهای مولکولی سرطان
در سطح مولکولی، سرطان نتیجه اختلال در مسیرهای سیگنالینگ سلولی است که کنترل رشد، تمایز و آپوپتوز سلولها را بر عهده دارند. جهشهای ژنتیکی در ژنهای آنکوژنها و ژنهای سرکوبکننده تومور، مانند RAS، TP53 و BRCA، میتوانند تعادل طبیعی بین رشد و مرگ سلولی را برهم بزنند. آنکوژنها ژنهایی هستند که در حالت طبیعی کنترل رشد سلولی را هدایت میکنند، اما در اثر جهش میتوانند فعالیت بیش از حد داشته و موجب تقسیم سلولی غیرطبیعی شوند. در مقابل، ژنهای سرکوبکننده تومور، مانند TP53، نقش محافظتی دارند و جهش در آنها باعث از دست رفتن کنترل سلولی میشود.
علاوه بر جهشهای ژنتیکی، اختلالات اپیژنتیکی مانند متیلاسیون DNA، تغییرات هیستونی و بیان غیرطبیعی RNAهای غیرکدکننده نیز میتوانند به ایجاد سرطان کمک کنند. این تغییرات بدون تغییر در توالی DNA، بیان ژنها را تغییر داده و مسیرهای سیگنالینگ سلولی را مختل میکنند. به عنوان مثال، افزایش متیلاسیون پروموتر ژنهای سرکوبکننده تومور میتواند باعث خاموشی آنها و تسریع رشد تومور شود.
ژنتیک و حساسیت فردی به سرطان
برخی افراد به دلیل پلیمورفیسمها و جهشهای ارثی، استعداد بیشتری برای ابتلا به سرطان دارند. به عنوان مثال، حاملان جهشهای BRCA1 و BRCA2 خطر ابتلا به سرطان پستان و تخمدان را به طور قابل توجهی افزایش میدهند. مطالعات اپیدمیولوژیک نشان میدهد که ترکیب ژنتیک فرد و عوامل محیطی میتواند به ایجاد سرطانهای پیچیده مانند سرطان روده بزرگ و کبد منجر شود. همچنین، پژوهشهای جدید در زمینه HERVs (Human Endogenous Retroviruses) نشان دادهاند که این عناصر ژنتیکی در برخی سرطانها فعال میشوند و میتوانند فرآیندهای التهابی و پروتومیک سلولی را تغییر دهند، که این یافتهها افق تازهای در درک پاتوژنز سرطان باز کرده است.
نقش سیستم ایمنی در پیشرفت سرطان
سیستم ایمنی نقش محافظتی حیاتی در شناسایی و حذف سلولهای سرطانی دارد. سلولهای T و NK میتوانند سلولهای غیرطبیعی را شناسایی و از بین ببرند، اما تومورها با ایجاد میکرو محیط ایمنی سرکوبکننده، مانند تولید سیتوکینهای ضد التهابی و جذب سلولهای تنظیمی T (Treg)، از حمله ایمنی فرار میکنند. این مکانیسمها توضیح میدهند که چرا برخی تومورها به درمانهای ایمنی پاسخ نمیدهند و نیازمند استراتژیهای نوین ایمنیدرمانی هستند. به عنوان مثال، در سرطان کبد، تعامل بین تومور و سلولهای ایمنی محیطی یکی از عوامل کلیدی مقاومت به درمان است.
میکروبیوم و سرطان
یکی از تازهترین یافتهها در زمینه سرطان، نقش میکروبیوم بدن در شروع و پیشرفت بیماری است. میکروبیوم روده، واژن و پوست میتواند بر فرآیندهای التهابی، مسیرهای سیگنالینگ و پاسخ به درمانهای ضدسرطان اثر بگذارد. مطالعات نشان دادهاند که عدم تعادل میکروبیوم روده میتواند خطر سرطان روده بزرگ را افزایش دهد، در حالی که تعامل HPV با میکروبیوتای واژن میتواند در سرطان گردن رحم نقش داشته باشد. این یافتهها نه تنها در تشخیص زودهنگام سرطان اهمیت دارند، بلکه در طراحی درمانهای هدفمند و پیشگیریهای نوین نیز کاربرد دارند.
مسیرهای سیگنالینگ و اهداف درمانی
درک مسیرهای سیگنالینگ سلولی، مانند مسیر Nrf2، YAP/TAZ و MAPK/PI3K، به توسعه درمانهای هدفمند کمک کرده است. این مسیرها میتوانند در پاسخ سلولی به استرس اکسیداتیو، تکثیر و مهاجرت سلولی نقش داشته باشند. برای نمونه، فعال شدن مسیر Nrf2 میتواند در برخی سرطانها به مقاومت دارویی منجر شود و در برخی دیگر اثر محافظتی داشته باشد. بنابراین، شناسایی و هدفگیری دقیق این مسیرها، کلید طراحی درمانهای نوین و شخصیسازیشده است.
عوامل محیطی و رفتاری در پایههای مولکولی سرطان
تغییرات مولکولی سرطان تنها نتیجه جهشهای ژنتیکی نیست؛ عوامل محیطی و سبک زندگی نیز میتوانند مسیرهای مولکولی و اپیژنتیکی را تغییر دهند. مصرف مواد شیمیایی مانند PFAS، مواجهه با فلزات سنگین و آلودگی هوا میتوانند باعث آسیب DNA و تغییرات اپیژنتیکی شوند. همچنین، رژیم غذایی نامناسب، کمتحرکی و استرس مزمن میتوانند پاسخ ایمنی را تضعیف کنند و زمینهساز رشد تومورها شوند. در مقابل، ترکیبات فیتوشیمیایی مانند کورکومین و رزوراترول مسیرهای سیگنالینگ ضدسرطانی را فعال میکنند و اثر حفاظتی در برابر برخی سرطانها دارند.
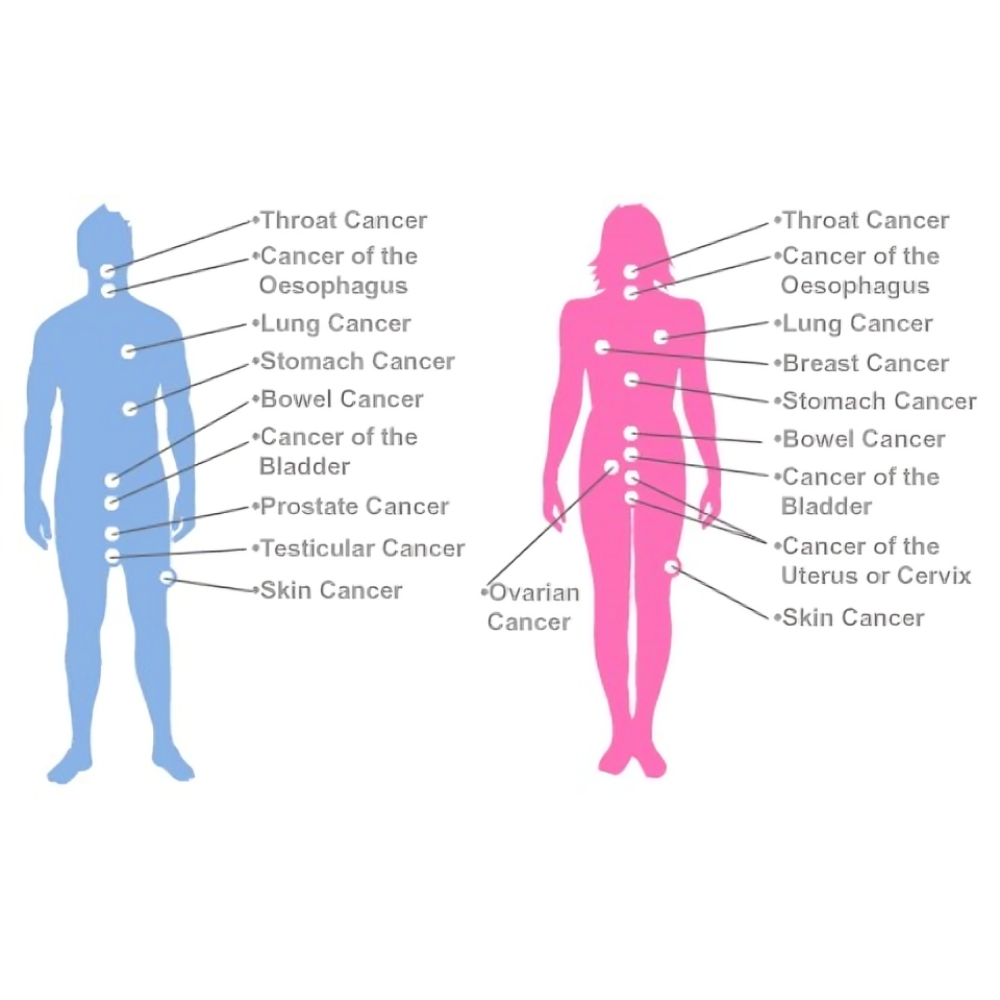
سرطانهای شایع در انسان و ویژگیهای آنها
سرطانهای شایع در انسان تنوع گستردهای دارند و هر یک ویژگیهای منحصر به فردی از نظر شیوع، عوامل زمینهای، مکانیسمهای مولکولی و پاسخ به درمان دارند. شناخت دقیق این ویژگیها نه تنها در تشخیص و درمان مؤثر است، بلکه میتواند در پیشگیری و غربالگری نیز راهگشا باشد. در ادامه، مهمترین سرطانهای شایع بررسی شدهاند.
سرطان پوست
سرطان پوست یکی از شایعترین انواع سرطانها در سطح جهان است و شامل انواع ملانوما، کارسینوم سلول بازال و کارسینوم سلول سنگفرشی میشود. میزان شیوع آن در مناطق با تابش شدید نور خورشید بالا است و فاکتورهای ژنتیکی، رنگ پوست، قرارگیری در معرض اشعه UV و سابقه آفتابسوختگی در ایجاد آن نقش دارند. ملانوما، اگرچه کمتر از سایر انواع پوست شایع است، اما به دلیل توانایی بالای متاستاز و مرگ و میر بالا اهمیت ویژهای دارد. تشخیص زودهنگام این سرطان از طریق معاینات پوستی و استفاده از بیوپسی و تکنیکهای تصویربرداری پیشرفته امکانپذیر است. درمانها شامل جراحی، رادیوتراپی و ایمنیدرمانی هستند و در سالهای اخیر، توسعه داروهای هدفمند و آنتیبادیها، چشمانداز درمان را بهبود بخشیده است.
سرطان پستان
سرطان پستان در زنان شایعترین سرطان است و یکی از علل اصلی مرگ ناشی از سرطان به شمار میآید. عوامل ریسک شامل ژنتیک (BRCA1/BRCA2)، سن، هورمونها، سبک زندگی و مواجهه با فلزات سنگین هستند. مواجهه با فلزات سنگین مانند کادمیوم و آرسنیک میتواند ریسک سرطان پستان را افزایش دهد و مکانیسم آن شامل استرس اکسیداتیو و اختلال مسیرهای سیگنالینگ سلولی است. تشخیص زودهنگام از طریق ماموگرافی، سونوگرافی و بیومارکرهای نوین انجام میشود. درمانها شامل جراحی، شیمیدرمانی، هورموندرمانی، هدفمند درمانی و ایمنیدرمانی هستند. تحقیقات اخیر نشان میدهند که نانوفرمولههای فیتوشیمیایی میتوانند اثرات حفاظتی و درمانی در سرطان پستان داشته باشند.
سرطان روده بزرگ
سرطان روده بزرگ، یکی از سرطانهای شایع دستگاه گوارش، با رژیم غذایی، سبک زندگی، میکروبیوم روده و عوامل ژنتیکی ارتباط دارد. مصرف غذاهای فرآوریشده و کمبود فیبر با افزایش ریسک این سرطان مرتبط است. میکروبیوم روده نقش مهمی در تنظیم پاسخهای التهابی و مسیرهای سیگنالینگ دارد و عدم تعادل آن میتواند منجر به تغییرات ژنتیکی و اپیژنتیکی سلولهای روده شود. پیشگیری شامل رژیم غذایی سالم، ورزش و غربالگری منظم با کولونوسکوپی است. درمانها بسته به مرحله سرطان شامل جراحی، شیمیدرمانی و درمان هدفمند با فیتوشیمیاییها مانند کورکومین و رزوراترول هستند.
سرطان کبد
سرطان کبد، به ویژه هپاتوسلولار کارسینوما، در کشورهای با شیوع بالای هپاتیت B و C و مواجهه با عوامل محیطی مانند آفلاتوکسینها و آلودگی هوا شایع است. میکرو محیط ایمنی کبد نقش مهمی در رشد تومور دارد و سلولهای ایمنی سرکوبکننده مانند Treg و ماکروفاژهای M2 میتوانند پاسخ ایمنی ضدسرطان را مهار کنند. درمانها شامل جراحی، پیوند کبد، ایمنیدرمانی و درمان هدفمند با داروهای مولکولی است. تحقیقات نوین بر روی ترکیب ایمنیدرمانی و درمان هدفمند تمرکز دارند تا اثربخشی درمان افزایش یابد.
سرطان دهان و حلق مرتبط با HPV
ویروس پاپیلومای انسانی (HPV) به عنوان عامل اصلی در برخی سرطانهای دهان، حلق و اوروفارنکس شناخته شده است. مکانیسم شامل ادغام DNA ویروسی با ژنوم سلول میزبان و اختلال در ژنهای سرکوبکننده تومور است. درمانها شامل جراحی، رادیوتراپی و ایمنیدرمانی هستند و مطالعات اخیر بر روی کاهش شدت درمان (deintensification) و بهبود کیفیت زندگی بیماران متمرکز شدهاند. واکسیناسیون علیه HPV نیز یکی از راهکارهای پیشگیری مؤثر محسوب میشود.
سرطان گردن رحم
سرطان گردن رحم به طور عمده با HPV و تغییرات میکروبیوتای واژن مرتبط است. بررسیهای اخیر نشان دادهاند که تعامل بین ویروس و میکروبیوم میتواند روند تبدیل سلولهای اپیتلیال به حالت پیشسرطانی و سپس سرطان را تسریع کند. پیشگیری شامل واکسیناسیون HPV، غربالگری با پاپ اسمیر و کولپوسکوپی است. درمانها شامل جراحی، شیمیدرمانی، رادیوتراپی و ایمنیدرمانی میشوند و تحقیقات نوین بر روی بیومارکرهای تشخیصی و درمان هدفمند تمرکز دارند.
سرطان مثانه و HPV
شواهد اخیر نشان میدهند که HPV ممکن است در برخی موارد سرطان مثانه نقش داشته باشد. مطالعات متاآنالیز و تحلیلهای ژنتیکی دو نمونهای، ارتباط بین عفونت HPV و افزایش ریسک این سرطان را تایید کردهاند. مکانیسمهای احتمالی شامل فعال شدن مسیرهای سیگنالینگ سرطانی و اختلال در کنترل رشد سلولی است. درمانها شامل سیستکتومی، شیمیدرمانی و ایمنیدرمانی هستند.
سرطانهای دیگر مرتبط با ویروسها و HERVs
علاوه بر HPV، سایر ویروسها مانند EBV، HBV، HCV و HERVs (Human Endogenous Retroviruses) میتوانند در ایجاد سرطانهای متنوع نقش داشته باشند. این ویروسها میتوانند مسیرهای التهابی و سیگنالینگ سلولی را تغییر داده و زمینهساز تکوین تومور شوند. بهطور مثال، HERVs در برخی سرطانهای خون و تومورهای جامد فعال میشوند و اثرات پروتومیک و ایمنیزیستشناسی قابل توجهی دارند.
عوامل محیطی و شغلی مرتبط با سرطان
سرطان نه تنها نتیجه تغییرات ژنتیکی و مولکولی است، بلکه عوامل محیطی و شغلی نقش مهمی در ایجاد و پیشرفت آن دارند. مواجهه طولانیمدت با مواد شیمیایی، فلزات سنگین، آلایندههای هوا و رفتارهای سبک زندگی ناسالم میتواند خطر ابتلا به سرطان را افزایش دهد. درک این عوامل برای پیشگیری، غربالگری و طراحی استراتژیهای درمانی حیاتی است.
مواد شیمیایی محیطی و سرطان
یکی از مهمترین عوامل محیطی، مواجهه با مواد شیمیایی است. مطالعات اخیر نشان دادهاند که PFAS (Per- and Poly-Fluoroalkyl Substances)، که در صنایع مدرن و محصولات مصرفی مانند ظروف تفلون، فومهای آتشنشانی و بستهبندیهای مواد غذایی یافت میشوند، میتوانند خطر ابتلا به سرطانهای گوارشی را افزایش دهند. مکانیسم این تأثیر شامل ایجاد استرس اکسیداتیو، اختلال در مسیرهای سیگنالینگ سلولی و جهشهای DNA است. علاوه بر PFAS، مواجهه با آلایندههای صنعتی و محصولات جانبی نفتی نیز با افزایش ریسک سرطانهای مختلف، به ویژه سرطان کبد و روده بزرگ، مرتبط است.
فلزات سنگین و سرطان
فلزات سنگین مانند کادمیوم، آرسنیک، سرب و جیوه از عوامل شغلی و محیطی شناخته شدهاند که میتوانند فرآیندهای سلولی را مختل کنند و منجر به سرطان شوند. به عنوان مثال، کادمیوم با اختلال در مسیرهای تولید رادیکالهای آزاد، استرس اکسیداتیو و تغییرات اپیژنتیک موجب افزایش خطر سرطان پستان و پروستات میشود. آرسنیک نیز از طریق تغییرات متیلاسیون DNA و اختلال در مسیرهای تنظیم رشد سلولی، در ایجاد سرطانهای پوستی و گوارشی نقش دارد. مواجهه طولانیمدت با این فلزات معمولاً در صنایع معدنی، فلزکاری و کشاورزی رخ میدهد و نیازمند کنترلهای بهداشتی و صنعتی دقیق است.
قرارگیری در معرض اشعه و نور خورشید
یکی دیگر از عوامل مهم محیطی، اشعه UV و دیگر انواع تابش یونیزان است. تابش مستقیم خورشید، به ویژه در طولانیمدت و بدون محافظت، میتواند باعث ایجاد جهشهای DNA و سرطان پوست شود. اشعههای یونیزان نیز در محیطهای شغلی خاص، مانند کار با دستگاههای رادیولوژی و هستهای، میتوانند ریسک سرطان را افزایش دهند. استفاده از محافظتهای فیزیکی و تجهیزات ایمنی در این محیطها برای پیشگیری از سرطان ضروری است.
سیگار، الکل و سبک زندگی
رفتارهای سبک زندگی نقش بسیار مهمی در ابتلا به سرطان دارند. سیگار کشیدن یکی از مهمترین عوامل محیطی است که با سرطانهای ریه، حنجره، مثانه و روده بزرگ ارتباط مستقیم دارد. الکل نیز میتواند از طریق ایجاد استرس اکسیداتیو و اختلال در متابولیسم فولات، ریسک سرطانهای کبد، دهان و گلو را افزایش دهد. کمتحرکی و رژیم غذایی ناسالم، مانند مصرف غذاهای فرآوریشده و کمفیبر، میتواند خطر سرطانهای روده بزرگ و پستان را افزایش دهد. به همین دلیل، اصلاح رفتارهای سبک زندگی یکی از مؤثرترین روشهای پیشگیری است.
عوامل شغلی و مواجهه طولانیمدت
برخی مشاغل مستعد افزایش مواجهه با عوامل سرطانزا هستند. کارگران صنایع شیمیایی، فلزکاری، معدن و ساختمانسازی ممکن است در معرض حلالها، فلزات سنگین، گرد و غبار و مواد آلی سرطانزا قرار گیرند. مطالعات نشان دادهاند که مواجهه طولانیمدت با این عوامل میتواند باعث ایجاد جهشهای ژنتیکی و تغییرات اپیژنتیک شود که زمینهساز انواع سرطانها میشوند. ایجاد سیستمهای کنترل محیطی، آموزش ایمنی و غربالگری شغلی منظم برای کاهش این ریسک ضروری است.
آلودگی هوا و سرطان
آلودگی هوا، به ویژه ذرات معلق (PM2.5 و PM10) و ترکیبات آلاینده مانند NOx، SOx و بنزن، با افزایش ریسک سرطانهای ریه و گوارش مرتبط است. مکانیسمهای مولکولی شامل ایجاد التهاب مزمن، استرس اکسیداتیو و آسیب DNA هستند. مطالعات جمعیتی نشان میدهند که مناطق با آلودگی هوای بالا، شیوع سرطانهای تنفسی بیشتری دارند و کاهش مواجهه با این آلایندهها میتواند نقش پیشگیرانه داشته باشد.
ترکیب عوامل محیطی و ژنتیک
تأثیر عوامل محیطی معمولاً به صورت مستقل نیست و با سازگاری ژنتیکی و اپیژنتیکی فرد تعامل دارد. برای مثال، فردی با جهش BRCA1 که در معرض فلزات سنگین قرار میگیرد، ممکن است ریسک بسیار بالاتری برای سرطان پستان داشته باشد نسبت به فردی بدون این جهش. این تعاملها نشان میدهند که پیشگیری و مدیریت سرطان نیازمند رویکردی جامع است که ژنتیک، محیط و سبک زندگی را در نظر بگیرد.
اهمیت پیشگیری و سیاستهای بهداشتی
با توجه به نقش گسترده عوامل محیطی و شغلی در سرطان، سیاستهای بهداشتی و صنعتی باید شامل محدودیتهای مواجهه با مواد شیمیایی، آموزش کارکنان، کاهش آلودگی هوا و ترویج سبک زندگی سالم باشد. غربالگری منظم و آگاهیبخشی عمومی نیز از ابزارهای مؤثر در کاهش بار سرطانها محسوب میشود.
روشهای تشخیص و پایش سرطان
تشخیص زودهنگام سرطان یکی از مهمترین عوامل در بهبود نرخ بقا و موفقیت درمان است. در سالهای اخیر، پیشرفتهای علمی و تکنولوژیک روشهای تشخیص را به سطحی رسانده است که علاوه بر شناسایی بیماری، امکان پایش پیشرفت تومور و پاسخ به درمان را نیز فراهم میکند. این بخش به بررسی کامل روشهای تشخیص سنتی و نوین، بیومارکرها و تکنولوژیهای بایوسنسینگ، تصویربرداری و نقش میکروبیوم میپردازد.
بیومارکرهای سرطان
بیومارکرها مولکولهایی هستند که میتوانند وجود سرطان، مرحله پیشرفت و پاسخ به درمان را نشان دهند. این مولکولها میتوانند شامل پروتئینها، DNA و RNA سرطانی، متابولیتها یا ترکیبات ایمنی باشند. بیومارکرها در انواع سرطانها، مانند سرطان پستان، روده بزرگ، گردن رحم و کبد مورد استفاده قرار میگیرند. به عنوان مثال، سطح CA-125 در خون برای پایش سرطان تخمدان استفاده میشود و PSA یک بیومارکر شناخته شده برای سرطان پروستات است.
علاوه بر این، بیومارکرهای مولکولی نوین مانند RNAهای غیرکدکننده، DNA آزاد سرطانی (cfDNA) و پروتئینهای اختصاصی، امکان تشخیص زودهنگام حتی قبل از ظهور علائم بالینی را فراهم کردهاند. این فناوریها به خصوص در سرطانهای مرتبط با HPV و سرطانهای گوارشی اهمیت دارند، زیرا میتوانند سلولهای پیشسرطانی و تغییرات مولکولی اولیه را شناسایی کنند.
تکنولوژیهای بایوسنسینگ
پیشرفت در بایوسنسورها و روشهای حسگری زیستی امکان تشخیص سریع و دقیق سرطانها را فراهم کرده است. این سیستمها با استفاده از آنتیبادیها، DNA پروبها و نانوذرات قادر به شناسایی بیومارکرهای اختصاصی هستند. به عنوان مثال، سنسورهای نانومقیاس میتوانند سطح cfDNA یا پروتئینهای سرطانی را در خون یا ادرار اندازهگیری کنند و در عرض چند ساعت اطلاعات تشخیصی ارائه دهند. تحقیقات نشان دادهاند که این روشها در تشخیص سرطان گردن رحم، پستان و روده بزرگ بسیار مؤثر هستند و قابلیت استفاده در غربالگری جمعیتی را دارند.
تصویربرداری و تکنیکهای مدرن
تصویربرداری یکی از ستونهای اصلی تشخیص و پایش سرطان است. روشهای مرسوم شامل رادیوگرافی، سیتی اسکن، امآرآی و اولتراسونوگرافی هستند که امکان بررسی ساختار و اندازه تومورها را فراهم میکنند. علاوه بر این، پت اسکن (PET Scan) و تصویربرداری مولکولی امکان بررسی فعالیت متابولیک سلولهای سرطانی را فراهم میکنند و برای پایش پاسخ به درمان و شناسایی متاستازها حیاتی هستند.
تکنیکهای جدید تصویربرداری نیز بر روی تصویربرداری چندمدلی و تصویربرداری مبتنی بر بیومارکرهای مولکولی تمرکز دارند. به عنوان مثال، آنتیبادیهای نشاندار شده با رادیونوکلئیدها میتوانند سلولهای سرطانی خاص را هدف قرار دهند و اطلاعات دقیقتری نسبت به روشهای سنتی ارائه کنند. این فناوریها امکان تشخیص سرطانهای اولیه و کوچکترین تومورها را فراهم میکنند، که پیش از این از دید روشهای سنتی پنهان میماند.
نقش میکروبیوم در تشخیص و پایش
مطالعات اخیر نشان دادهاند که میکروبیوم بدن، به ویژه روده، واژن و پوست، میتواند به عنوان بیومارکر غیرمستقیم در تشخیص سرطانها استفاده شود. تغییرات ترکیب میکروبیوتا، مانند کاهش گونههای مفید یا افزایش باکتریهای التهابی، با سرطانهای روده بزرگ، گردن رحم و پوست مرتبط است. بررسی میکروبیوم به کمک تکنیکهای توالییابی نسل جدید (NGS) و متاژنومیکس امکان شناسایی الگوهای اختصاصی مرتبط با سرطان را فراهم کرده و میتواند به عنوان ابزار پیشبینی کننده پیشرفت بیماری و پاسخ به درمان مورد استفاده قرار گیرد.
تشخیص ترکیبی و شخصیسازی شده
امروزه، ترکیب روشهای مختلف تشخیصی، از جمله بیومارکرهای مولکولی، بایوسنسورها، تصویربرداری مدرن و بررسی میکروبیوم، بهترین رویکرد برای تشخیص و پایش سرطان محسوب میشود. این روشها امکان تشخیص زودهنگام، پایش دقیق پیشرفت تومور و ارزیابی پاسخ به درمان را فراهم میکنند و میتوانند به طراحی درمانهای شخصیسازی شده و هدفمند کمک کنند.
پایش درمان و پیشبینی پاسخ به درمان
یکی از کاربردهای مهم این روشها، ارزیابی اثربخشی درمان و پیشبینی پاسخ بیماران به روشهای مختلف درمانی است. به عنوان مثال، کاهش سطح cfDNA یا تغییرات بیومارکری در خون میتواند نشاندهنده پاسخ موفق به شیمیدرمانی یا ایمنیدرمانی باشد. همچنین، بررسی میکروبیوم میتواند به پیشبینی عوارض جانبی درمانهای شیمیایی و ایمنیدرمانی کمک کند و به تنظیم دقیقتر برنامه درمانی بیماران منجر شود.
درمانهای نوین سرطان
با پیشرفت علم و فناوری، درمان سرطان از روشهای سنتی مانند جراحی، شیمیدرمانی و رادیوتراپی به سمت درمانهای نوین، هدفمند و شخصیسازیشده حرکت کرده است. این درمانها با تمرکز بر مکانیسمهای مولکولی، مسیرهای سیگنالینگ و تعامل تومور با سیستم ایمنی، تلاش میکنند تا اثرات جانبی کاهش یابد و اثربخشی درمان افزایش یابد.
درمانهای هدفمند
درمان هدفمند بر اساس اختلالات مولکولی خاص سلولهای سرطانی طراحی شده است. این داروها مسیرهای سیگنالینگ غیرطبیعی، آنکوژنها و ژنهای سرکوبکننده تومور را هدف قرار میدهند. به عنوان مثال، مهارکنندههای تیروزین کیناز (TKI) در سرطان ریه و برخی سرطانهای گوارشی استفاده میشوند و با مهار مسیرهای رشد سلولی، تکثیر تومور را کاهش میدهند.
درمانهای هدفمند همچنین شامل آنتیبادیهای مونوکلونال هستند که به پروتئینهای سطح سلول سرطانی متصل میشوند و باعث فعال شدن سیستم ایمنی یا مسدود کردن مسیرهای سیگنالینگ میشوند. این روشها در سرطانهای پستان، خون و معده کاربرد دارند و تحقیقات جدید بر روی ترکیب آنتیبادیها با داروهای شیمیدرمانی جهت افزایش اثربخشی و کاهش مقاومت دارویی متمرکز است.
ایمنیدرمانی سرطان
ایمنیدرمانی یکی از پیشرفتهترین حوزههای درمان نوین است و بر تقویت سیستم ایمنی بیمار برای شناسایی و نابودی سلولهای سرطانی تمرکز دارد. این روش شامل مهارکنندههای نقطهای (Checkpoint inhibitors)، سلولهای CAR-T و واکسنهای ضدسرطان است.
-
مهارکنندههای نقطهای مانند داروهای ضد-PD-1 و ضد-CTLA-4 میتوانند بلوک ایمنی ایجاد شده توسط تومورها را رفع کنند و پاسخ سلولهای T علیه سلولهای سرطانی را تقویت کنند. این درمانها در سرطانهای کبد، ریه و پوست اثربخشی قابل توجهی داشتهاند.
-
سلولهای CAR-T شامل سلولهای T اصلاحشده ژنتیکی هستند که گیرندههای خاصی برای شناسایی سلولهای سرطانی دارند و پس از بازگرداندن به بدن، توانایی حمله مستقیم به تومورها را پیدا میکنند. این روش در برخی سرطانهای خون و لنفوم نتایج موفقیتآمیزی داشته است.
-
واکسنهای ضدسرطان به ویژه در سرطانهای مرتبط با ویروسها مانند HPV و HBV کاربرد دارند و میتوانند با تحریک پاسخ ایمنی پیشگیرانه یا درمانی، پیشرفت بیماری را کنترل کنند.
درمانهای مبتنی بر فیتوشیمیاییها
ترکیبات طبیعی گیاهی، مانند کورکومین، رزوراترول و فیتوشیمیاییهای میوهها و سبزیجات، اثرات ضدسرطانی متعددی دارند. این ترکیبات میتوانند مسیرهای سیگنالینگ پروتومیک و ژنتیکی سلولهای سرطانی را تعدیل کرده، آپوپتوز را تحریک کرده و رشد تومور را کاهش دهند. مطالعات نشان دادهاند که ترکیبات فیتوشیمیایی میتوانند در پیشگیری و درمان سرطانهای روده بزرگ، پستان و پروستات نقش مؤثری ایفا کنند.
پیشرفتهای اخیر امکان نانوفورموله کردن فیتوشیمیاییها را فراهم کرده است. این روش باعث افزایش حلالیت، جذب سلولی و هدفگیری دقیق تومورها میشود و اثرات جانبی را کاهش میدهد. به عنوان مثال، نانوکورکومین در مطالعات پیشبالینی نشان داده است که میتواند مسیرهای Nrf2 و YAP/TAZ را هدف قرار داده و پاسخ سلولهای سرطانی را به درمان افزایش دهد.
درمان ترکیبی و شخصیسازیشده
یکی از ویژگیهای برجسته درمانهای نوین، ترکیب روشها و شخصیسازی درمان بر اساس ویژگیهای مولکولی تومور و بیمار است. برای مثال، ترکیب ایمنیدرمانی با داروهای هدفمند یا فیتوشیمیاییها میتواند اثرات ضدتوموری را افزایش دهد و مقاومت دارویی را کاهش دهد. همچنین، استفاده از بیومارکرها و تصویربرداری پیشرفته امکان پایش پاسخ درمان و تنظیم دقیقتر دوز داروها را فراهم میکند.
چالشها و چشمانداز آینده
با وجود پیشرفتهای چشمگیر، درمانهای نوین با چالشهایی مانند مقاومت دارویی، عوارض جانبی ایمنی و هزینههای بالا مواجه هستند. تحقیقات جاری بر روی پیشبینی پاسخ درمان، توسعه بیومارکرهای جدید و طراحی ترکیبهای درمانی بهینه متمرکز است. هدف نهایی، دستیابی به درمانهای کارآمد، با عوارض جانبی حداقل و شخصیسازی شده برای هر بیمار است.
چالشها و چشمانداز آینده در سرطان
با وجود پیشرفتهای چشمگیر در تشخیص، پایش و درمان سرطان، هنوز چالشهای بسیاری در مسیر مدیریت این بیماری وجود دارد. این چالشها شامل محدودیتهای تکنولوژیک، مقاومت دارویی، پیچیدگی مولکولی تومورها و مشکلات اقتصادی و اجتماعی هستند. در این بخش، این چالشها بررسی شده و چشماندازهای نوآورانه برای غلبه بر آنها ارائه میشود.
مقاومت دارویی و محدودیت درمانهای نوین
یکی از بزرگترین چالشها در درمان سرطان، مقاومت دارویی است. سلولهای سرطانی قادرند با تغییر مسیرهای سیگنالینگ، فعالسازی مکانیزمهای بازسازی DNA و تغییر میکرو محیط تومور، مقاومت نسبت به داروهای شیمیدرمانی، هدفمند و ایمنیدرمانی ایجاد کنند. به عنوان مثال، در برخی سرطانهای ریه و روده بزرگ، سلولها با فعال شدن مسیرهای جایگزین، از مهارکنندههای تیروزین کیناز فرار میکنند. مقابله با مقاومت دارویی نیازمند ترکیب درمانها، تغییر دوز داروها و توسعه داروهای جدید با مکانیسمهای متفاوت است.
چالشهای ایمنیدرمانی
با وجود موفقیتهای ایمنیدرمانی، این روشها با عوارض جانبی ایمنی و پاسخ متغیر بیماران همراه هستند. برخی بیماران دچار واکنشهای التهابی شدید، آسیب به بافتهای سالم و سندرمهای ایمنی خودکار میشوند. علاوه بر این، برخی تومورها با ایجاد محیط ایمنی سرکوبکننده، پاسخ به ایمنیدرمانی را کاهش میدهند. تحقیقات آینده بر روی بیومارکرهای پیشبینیکننده پاسخ و طراحی ترکیبهای ایمنیدرمانی شخصیسازیشده تمرکز دارد تا این مشکلات کاهش یابد.
پیچیدگی مولکولی تومورها و تنوع ژنتیکی
تومورهای انسانی اغلب دارای تنوع ژنتیکی و اپیژنتیکی بالا هستند، که باعث میشود یک درمان برای همه بیماران مؤثر نباشد. به عنوان مثال، سرطانهای پستان یا روده بزرگ میتوانند در بیماران مختلف با جهشها و مسیرهای سیگنالینگ متفاوت ظاهر شوند. این پیچیدگی نیازمند تشخیص دقیق مولکولی، بیومارکرهای اختصاصی و شخصیسازی درمان است تا اثرات درمانی حداکثر شود.
دسترسی و مسائل اقتصادی درمان
یکی دیگر از چالشهای مهم، دسترسی محدود بیماران به درمانهای پیشرفته و هزینه بالای درمانهای نوین است. ایمنیدرمانی، درمانهای هدفمند و نانوفرمولهها اغلب بسیار گران هستند و در کشورهای با منابع محدود، بیماران ممکن است از مزایای آن محروم باشند. ایجاد سیاستهای بهداشتی مناسب، حمایت دولتی و کاهش هزینههای تولید دارو، از راهکارهای کاهش این چالش محسوب میشوند.
چشمانداز آینده در مدیریت سرطان
با پیشرفت علم، چشمانداز آینده در سرطان شامل چند محور کلیدی است:
-
پیشگیری و غربالگری پیشرفته: استفاده از بیومارکرهای مولکولی، تحلیل میکروبیوم و تکنیکهای بایوسنسینگ امکان تشخیص زودهنگام و پیشگیری هدفمند را فراهم میکند.
-
شخصیسازی درمان: طراحی درمانها بر اساس ویژگیهای ژنتیکی و مولکولی بیمار، ترکیب درمانهای هدفمند و ایمنیدرمانی و استفاده از فیتوشیمیاییهای نانوفورموله، باعث افزایش اثربخشی و کاهش عوارض میشود.
-
ترکیب درمانها و نوآوریهای مولکولی: ترکیب روشهای نوین با درمانهای سنتی، استفاده از آنتیبادیها، مهارکنندههای مسیرهای سیگنالینگ و درمانهای مبتنی بر RNA میتواند مقاومت دارویی را کاهش دهد.
-
فناوریهای دیجیتال و هوش مصنوعی: استفاده از الگوریتمهای یادگیری ماشینی و هوش مصنوعی در تحلیل دادههای مولکولی، تصویربرداری و پایش بیماران، امکان پیشبینی بهتر پاسخ درمان و تصمیمگیری بالینی دقیقتر را فراهم میکند.
-
افزایش همکاری جهانی و دسترسی عادلانه: توسعه داروها و روشهای درمانی با هزینه کمتر، آموزش پزشکان و اطلاعرسانی عمومی، به کاهش نابرابریهای درمانی کمک خواهد کرد.
نتیجهگیری بخش چالشها و چشمانداز آینده
با وجود چالشهای متعدد، پیشرفتهای علمی و تکنولوژیک نویدبخش بهبود کیفیت زندگی بیماران، افزایش نرخ بقا و کاهش مرگ و میر ناشی از سرطان است. ترکیب روشهای پیشگیری، تشخیص زودهنگام، درمانهای نوین و سیاستهای بهداشتی مناسب میتواند بار بیماری را به شکل قابل توجهی کاهش دهد.
جمعبندی و نتیجهگیری
سرطان به عنوان یکی از پیچیدهترین و مرگبارترین بیماریهای انسانی، همچنان یکی از چالشهای اصلی سلامت جهانی است. بررسی جامع عوامل مولکولی، محیطی، شغلی و سبک زندگی نشان میدهد که تأثیر این عوامل در ایجاد، پیشرفت و پاسخ به درمان سرطان بسیار قابل توجه است.
درک مولکولی و زیستشناسی سرطان
مطالعات در زمینه سرطانشناسی مولکولی نشان دادهاند که تغییرات ژنتیکی، اپیژنتیکی و اختلال در مسیرهای سیگنالینگ سلولی، پایه ایجاد تومورها را تشکیل میدهند. پروتئینهای آنکوژن، ژنهای سرکوبگر تومور و مسیرهای مانند YAP/TAZ و Nrf2 نقش تعیینکنندهای در رشد، متاستاز و مقاومت سلولهای سرطانی دارند. این دانش پایه، مسیر توسعه درمانهای هدفمند و ایمنیدرمانی را فراهم کرده و امکان پیشگیری و پایش دقیق را ایجاد کرده است.
سرطانهای شایع و ویژگیهای آنها
شناخت انواع سرطانهای شایع مانند سرطان پستان، روده بزرگ، کبد، پوست و گردن رحم، همراه با تحلیل عوامل ژنتیکی و محیطی آنها، برای طراحی استراتژیهای درمانی و پیشگیری ضروری است. سرطانهای مرتبط با ویروسها، به ویژه HPV، نشان میدهند که عوامل عفونی نیز نقش تعیینکنندهای در کارسینوژنز دارند و واکسیناسیون میتواند به عنوان ابزار پیشگیری مؤثر مورد استفاده قرار گیرد.
عوامل محیطی و شغلی
تحقیقات متعدد تأکید میکنند که مواد شیمیایی، فلزات سنگین، آلودگی هوا، اشعه UV، سیگار و الکل از عوامل محیطی و شغلی مهم در ایجاد سرطان هستند. مواجهه طولانیمدت با این عوامل میتواند باعث ایجاد جهشهای ژنتیکی، استرس اکسیداتیو و تغییرات اپیژنتیک شود. کنترل محیطی، آموزش ایمنی و اصلاح سبک زندگی ابزارهای مؤثر در پیشگیری از سرطان محسوب میشوند.
تشخیص و پایش سرطان
پیشرفتهای تکنولوژیک، از جمله بیومارکرهای مولکولی، بایوسنسورها، تصویربرداری پیشرفته و بررسی میکروبیوم، امکان تشخیص زودهنگام، پایش دقیق تومورها و ارزیابی پاسخ به درمان را فراهم کردهاند. ترکیب این روشها، همراه با تحلیل ژنتیکی و مولکولی، مسیر را برای پیشگیری و درمان شخصیسازیشده هموار کرده است.
درمانهای نوین و نوآوریها
درمانهای نوین سرطان، شامل درمانهای هدفمند، ایمنیدرمانی، ترکیبات فیتوشیمیایی نانوفورموله و ترکیبهای درمانی شخصیسازیشده، امکان افزایش اثربخشی و کاهش عوارض جانبی را فراهم کردهاند. این درمانها بهویژه در مقابله با مقاومت دارویی و پاسخ نامناسب بیماران کاربرد دارند و نشان میدهند که درمان سرطان نیازمند رویکرد جامع و مولکولی است.
چالشها و چشمانداز آینده
با وجود موفقیتهای درمانی، چالشهایی مانند مقاومت دارویی، پیچیدگی مولکولی تومورها، عوارض ایمنی و هزینههای بالای درمانهای نوین همچنان وجود دارند. چشمانداز آینده بر پیشگیری پیشرفته، تشخیص زودهنگام، شخصیسازی درمان، فناوریهای دیجیتال و هوش مصنوعی، و افزایش دسترسی جهانی متمرکز است. همگرایی این رویکردها نویدبخش بهبود کیفیت زندگی بیماران و کاهش بار سرطانها در سطح جهانی است.
نتیجهگیری نهایی
سرطان یک بیماری پیچیده و چندعاملی است که ژنتیک، محیط، سبک زندگی و عوامل عفونی در ایجاد و پیشرفت آن نقش دارند. پیشرفتهای علمی در زمینه تشخیص مولکولی، پایش بیومارکری و درمانهای نوین هدفمند و ایمنیدرمانی، امکان مدیریت بهتر بیماری را فراهم کردهاند. برای دستیابی به نتایج بهتر، ترکیب پیشگیری، تشخیص زودهنگام و درمان شخصیسازیشده ضروری است.
در نهایت، آینده مبارزه با سرطان بر پایه تحقیقات مولکولی پیشرفته، فناوریهای نوین تشخیصی و درمانی، و سیاستهای بهداشتی جامع شکل خواهد گرفت. این رویکرد جامع میتواند بار بیماری را کاهش داده، نرخ بقا را افزایش دهد و کیفیت زندگی بیماران را به شکل چشمگیری بهبود بخشد..