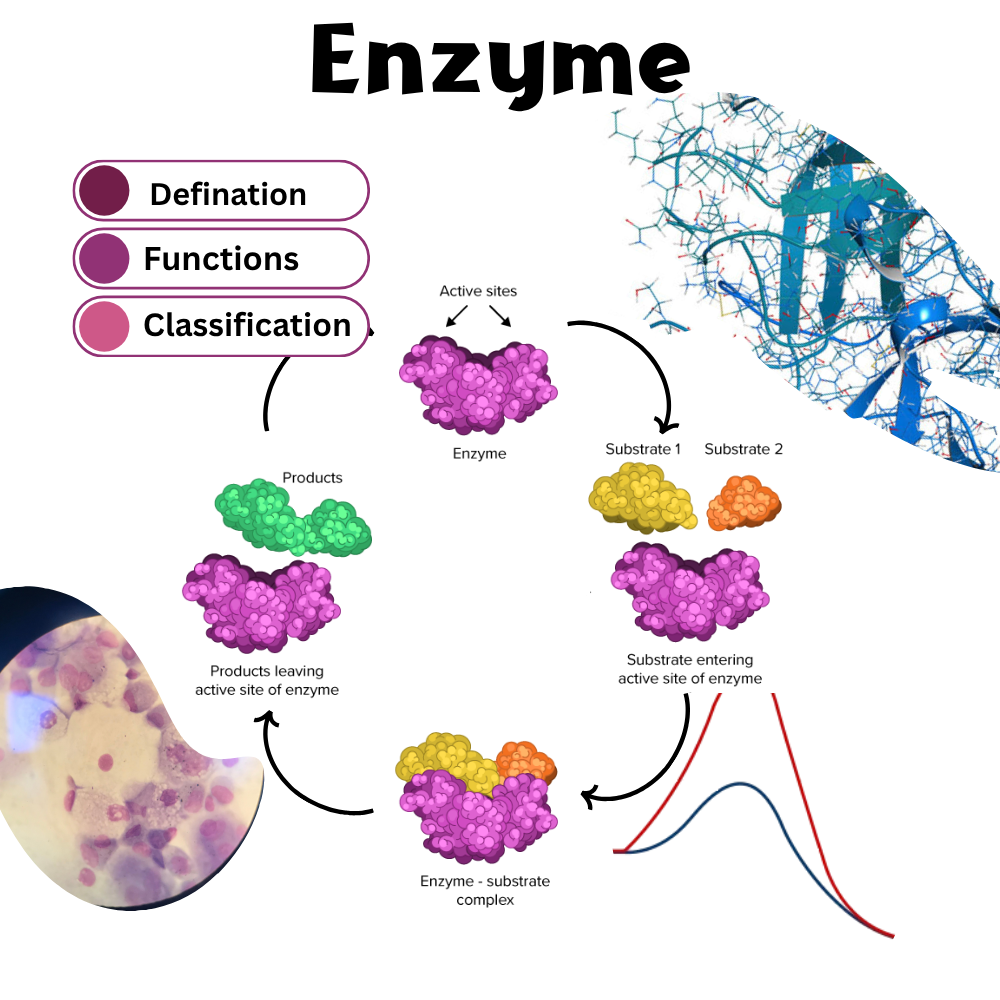
چرا واکسنهای mRNA توجه پژوهشگران را جلب کردهاند؟
واکسنهای شخصیشده mRNA برای سرطان: مسیر نوین درمانی و چشمانداز آینده
خلاصه
تصور کنید بدن انسان مانند یک شهر پیچیده و پرجمعیت استa، با میلیونها ساختمان (سلول) که هر یک وظایف ویژهای دارند. حال تصور کنید یکی از این ساختمانها یا مجموعهای از آنها به ناگاه شروع به ساخت دیوارها و سازههای خطرناک میکند: تومور.
واکسن شخصیشده بر پایه mRNA درست مانند ارسال پیامی اختصاصی به نیروهای حفاظتی شهر (سیستم ایمنی) عمل میکند: شناسایی و تخریب سلولهای سرطانی بدون آسیب رساندن به بافت سالم اطراف.
در این مقاله، با تجربه یکی از بازماندگان سرطان پانکراس آشنا میشویم و بررسی میکنیم که آیا این دستاورد علمی میتواند برای صدها هزار بیمار دیگر تکرار شود و چه موانع علمی، فناورانه و سیاسی در مسیر آن وجود دارد.
یک داستان واقعی: نجات با دوزهای شخصی
در پاییز ۲۰۲۰، پس از برداشت تومور لوزالمعده خانم باربارا بریگهم، مسیر نمونهبرداری و تحلیل بافت او آغاز شد: از انجماد در دمای ۸۰– درجه تا برشهای فوقالعاده نازک، رنگآمیزی و بررسی میکروسکوپی. بیش از ۵۰ محقق بر دقت این فرآیند نظارت داشتند.
دو ماه بعد، بریگهم به بیمارستان بازگشت تا واکسنی دریافت کند که اختصاصاً برای تومور او طراحی شده بود. این واکسن mRNA شامل دستورالعملهای ژنتیکی در نانوذرات چربی بود و به سیستم ایمنی میگفت: «این پروتئینها متعلق به تومور هستند؛ آنها را هدف قرار بده.»
چهار سال پس از آن، بریگهم در سلامت زندگی میکند و هیچ نشانهای از سرطان یا عوارض جدی درمان باقی نمانده است. اما پرسش اصلی همچنان باقی است: آیا میتوان این موفقیت شخصی را برای جمعیت وسیع بیماران تکرار کرد؟
چرا سیستم ایمنی اغلب تومور را نمیبیند؟
سیستم ایمنی معمولاً عوامل بیگانه مانند ویروسها و باکتریها را شناسایی میکند، اما سرطان پیچیدهتر است:
-
تومورها از سلولهای خود بدن شکل میگیرند؛ بنابراین سیستم ایمنی ممکن است آنها را «خودی» تلقی کند.
-
برخی تومورها بافتی شبیه سپر (استروما) ایجاد میکنند تا مانع دسترسی سلولهای ایمنی شوند.
-
تومورها سیگنالهای «چکپوینت» (checkpoint) تولید میکنند که مانع فعالیت سلولهای T میشوند.
پیش از دهههای ۱۹۹۰ و ۲۰۰۰، درمان سرطان عمدتاً شامل جراحی، پرتودرمانی یا شیمیدرمانی بود که سلولهای سالم و سرطانی را با هم هدف میگرفتند و عوارض زیادی داشتند.
با معرفی مهارکنندههای چکپوینت، مشخص شد سیستم ایمنی میتواند تومور را شناسایی کند، اما تنها حدود ۲۰٪ بیماران پاسخ مؤثری دریافت میکردند.
نئوآنتیژنها: نشانههای نامرئی تومور
سرطان با جهشهای ژنتیکی، پروتئینهای جدید و غیرمعمول تولید میکند که «نئوآنتیژن» نامیده میشوند، مانند پلاک خودرویی با شمارهای متفاوت.
-
برخی نئوآنتیژنها ناشی از جهشهای «راننده» (driver) هستند، مانند جهش KRAS در سرطان پانکراس. اغلب این آنتیژنها برای تحریک سیستم ایمنی کافی نیستند.
-
در بازماندگان طولانیمدت، بیشترین پاسخ ایمنی به آنتیژنهای «مسافر» (passenger) تعلق داشت؛ جهشهای تصادفی که معمولاً نادیده گرفته میشوند.
انتخاب آنتیژن مناسب، بهویژه در تومورهایی با تعداد جهش زیاد، مانند ملانوما، بهمثابه یافتن سوزن در انبار کاه است. در سرطان پانکراس با تعداد جهش کمتر، این انتخاب سادهتر و موفقیت محتملتر است.
mRNA : سکوی نوین برای واکسنهای شخصیشده
پلتفرم mRNA، برخلاف واکسنهای سنتی، تنها بخشی از کد ژنتیکی را منتقل میکند:
-
طراحی سریع: کافی است بخش mRNA حاوی نئوآنتیژن تغییر یابد.
-
انعطافپذیری: امکان ساخت واکسن اختصاصی برای هر بیمار وجود دارد.
-
تجربه موفق کووید-۱۹ نشان داد این پلتفرم قابل اعتماد، سریع و ایمن است.
شرکتهایی مانند BioNTech و Moderna اکنون روی واکسنهای mRNA برای سرطانهای مختلف، از جمله پانکراس، فعالیت میکنند.
چالش تولید: از تولید انبوه تا ویالهای شخصی
واکسن mRNA برای سرطان باید برای هر بیمار بهصورت اختصاصی ساخته شود:
-
نیاز به حجم اندک و زمان تولید کوتاه (چند هفته).
-
فرآیند کامل شامل تهیه مواد اولیه، پر کردن ویال و کنترل کیفیت باید سریع، دقیق و ایمن باشد.
-
اتوماسیون، رباتیک و هوش مصنوعی در آزمایشها و کنترل کیفیت به کار گرفته میشوند.
موانع مالی و سیاسی
-
کاهش بودجه تحقیقات سرطان در برخی کشورها مانع توسعه پروژهها است.
-
واکسنستیزی یا بیاعتمادی عمومی نیز تهدیدی برای گسترش این روش محسوب میشود.
-
هزینه بالای تولید واکسن شخصیشده بدون حمایت دولتی و عمومی، محدودیت ایجاد میکند.
چشمانداز آینده
اگر موانع رفع شوند:
-
واکسنهای شخصی mRNA ممکن است برای سرطانهایی مانند پانکراس، کلیه، مثانه و ریه عرضه شوند.
-
امکان مهار تومورها قبل از جراحی یا تولید واکسن پیشگیرانه وجود دارد.
-
سرمایهگذاری در تولید انبوه و آزمایش بالینی، مسیر تبدیل این پژوهشها به درمان واقعی را هموار میکند.
کلید موفقیت، پایداری مالی، حمایت اجتماعی و پژوهش مداوم است. میلیونها بیمار منتظرند روزی واکسنی اختصاصی دریافت کنند که سیستم ایمنیشان را برای دفاع فعالانه آماده سازد.
نتیجهگیری
واکسن شخصیشده mRNA، همانند طراحی کلیدی اختصاصی برای هر بیمار است: کلیدی که جهشهای دقیق تومور را میشناسد و سیستم ایمنی را برای حمله هدفمند فعال میکند. این فناوری تلفیقی از زیستشناسی مولکولی، هوش مصنوعی، مهندسی دارو و آرزوی دیرینه بشر برای شکست سرطان است؛ آرزویی که با حمایت مناسب، به زودی ممکن است تحقق یابد.
منابع و توضیحات:
https://www.scientificamerican.com/article/personalized-mrna-vaccines-will-revolutionize-cancer-treatment-if-federal